En Belgique, le premier essai clinique avec un médicament contenant un OGM a été notifié en 1996. Il s’agissait d’un essai de thérapie génique avec un virus Herpes simplex recombinant développé pour le traitement de cancers. 347 essais cliniques ont été notifiés entre 1996 et 2025, en large majorité pour usage humain (95%). 54% de tous les essais ont été notifiés uniquement dans le cadre de la procédure « utilisation confinée », 44% dans les cadres des procédures « utilisation confinée » et « dissémination volontaire », et seulement 2% uniquement dans le cadre de la procédure « dissémination volontaire ». Les essais cliniques sont notifiés en moyenne sur 2 sites.
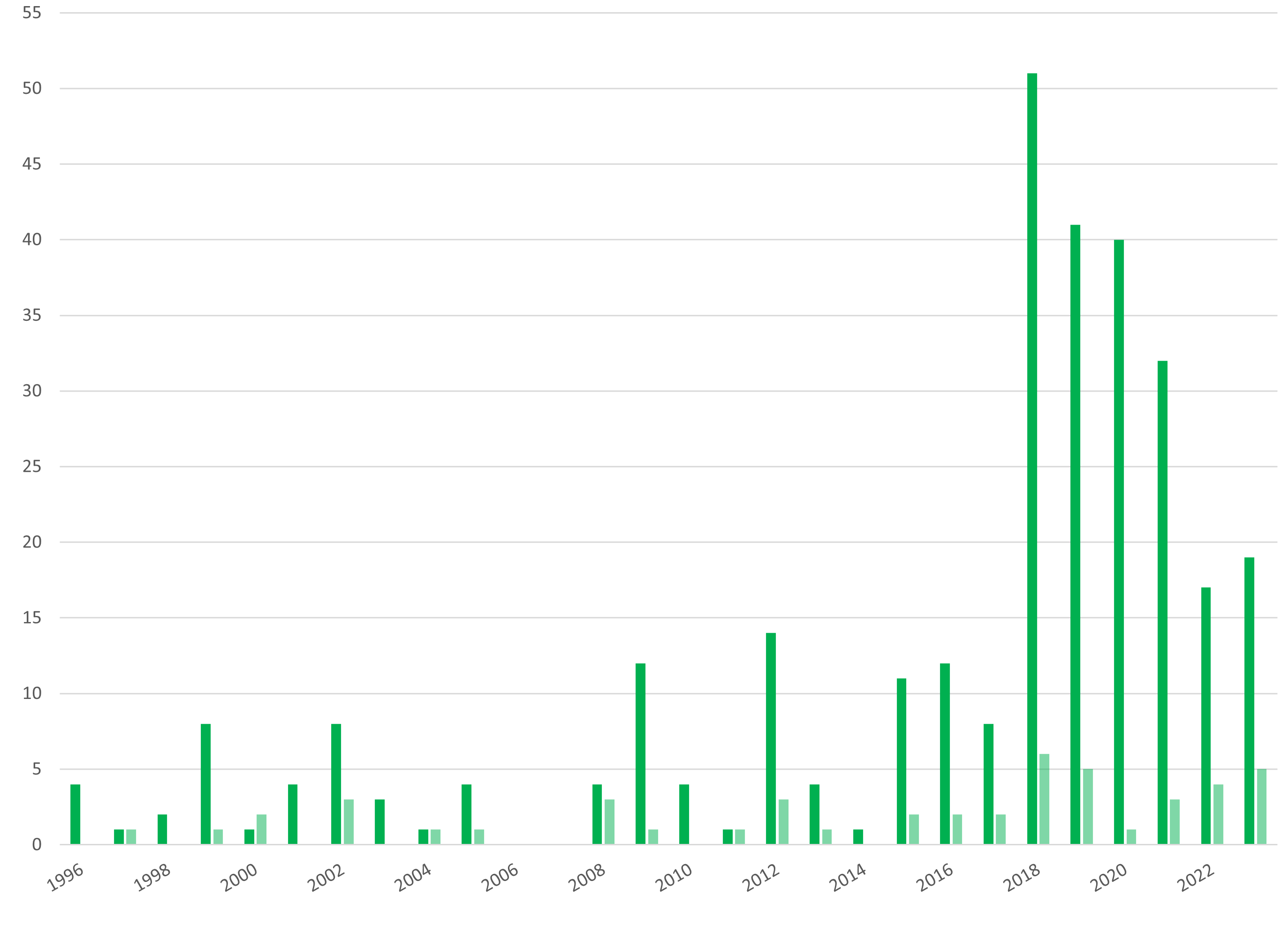
Nombre d’essais cliniques en Belgique mettant en œuvre des médicaments OGM destinés à l’homme, entre 1996 et 2025. Vert foncé : nombre d'avis remis concernant des essais cliniques notifiés selon la procédure « utilisation confinée » ; vert clair : nombre d'avis remis concernant des essais cliniques notifiés selon la procédure « dissémination volontaire ».
Le médicament expérimental OGM est un vecteur viral recombinant dans 61% des cas (employant principalement des virus dérivés de vaccinia, des adénovirus et des AAV), des cellules OGM dans 32% des cas, et d’autres MGM (comme des bactéries) dans 7% des cas. La grande majorité des essais ont pour but le traitement du cancer (55%), suivi de maladies infectieuses (26%). L’approche thérapeutique est majoritairement l’immunothérapie (50%), suivi de la prévention (24%) et la thérapie génique (20%).
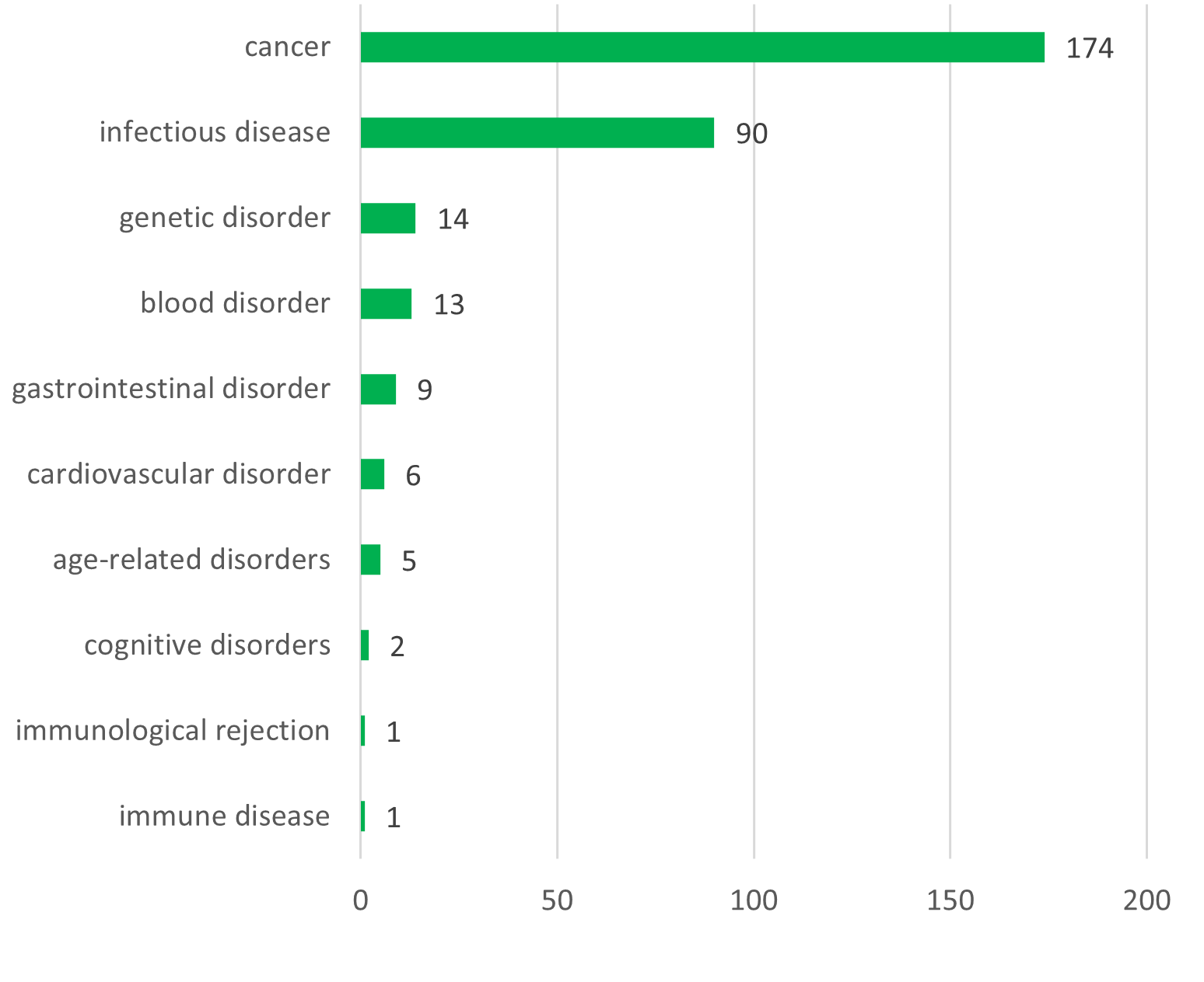
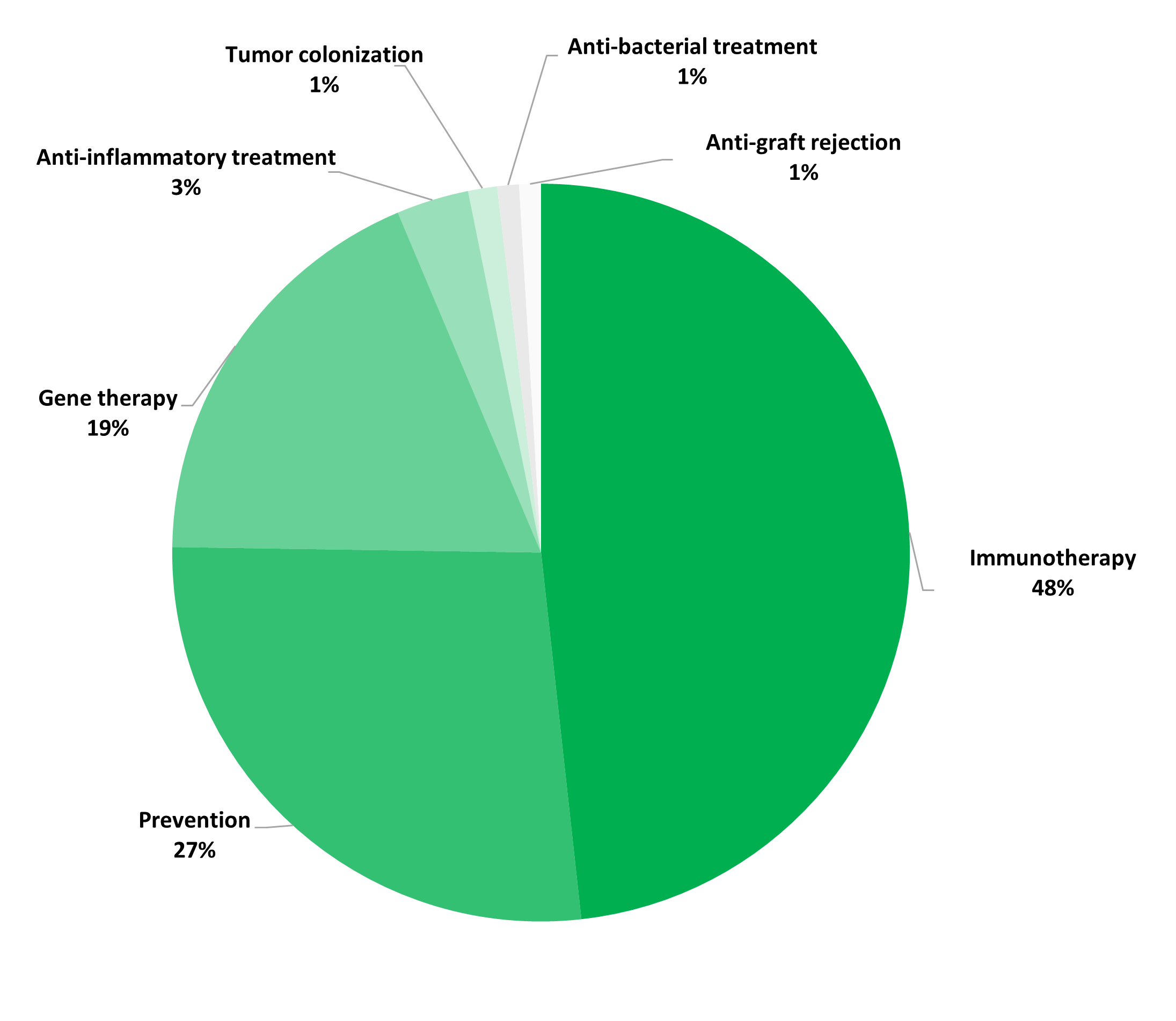
Indications (haut) et approches thérapeutiques (bas) pour les médicaments expérimentaux employés dans les essais cliniques (N = 357)
Pour plus d’informations et des descriptions détaillées sur chaque essai clinique, veuillez consulter notre base de données.
